风传8公里!禽流感空气传播惊现铁证,全球农场防控面临颠覆性挑战!

新研究揭示了风可能如何携带 H5N1 病毒在农场间传播,挑战了先前的假设并重塑了疫情预防策略。
近日发布于预印本平台 bioRxiv 的一项研究中,研究人员通过遗传学证据提出高致病性禽流感(HPAI)H5N1 病毒可能通过风进行远距离传播。尽管禽流感的风媒传播理论早有讨论,但实际记录案例仍十分罕见,且此前空气采样研究通常仅在感染农场约 150 米范围内检测到病毒。这项研究为远距离风媒传播提供了有力支持,但并未声称能完全证实这一机制。

研究背景
家禽农场是重要的空气污染物排放源。污染物在大小、形态和来源上存在差异,但通常包括液滴、气体及有机与无机颗粒。在 HPAI 疫情期间,禽类市场或农场内部的空气和灰尘中可检测到病毒颗粒。虽然空气传播是禽类间的主要感染方式,但受污染空气可能加剧疾病传播。研究还强调,机械通风的禽舍可能通过吸入周围污染空气而增加暴露风险,即使在低病毒浓度下也可能促进感染。
风长期以来被认为与甲型流感病毒(IAV)的远距离传播有关,但关于此传播方式的实地报告极少。尽管如此,采样研究已在感染农场 150 米外检测到 IAV,其病毒载量和阳性率较低,表明病毒载量与距离呈负相关。然而,在特定气象条件下,风媒传播可能跨越更远距离。
研究及发现
后院家禽作为病毒储存库——研究在鸭场附近的后院禽群中检测到遗传相似的 H5N1 毒株,表明野生鸟类可能助长了病毒在当地的持续传播。
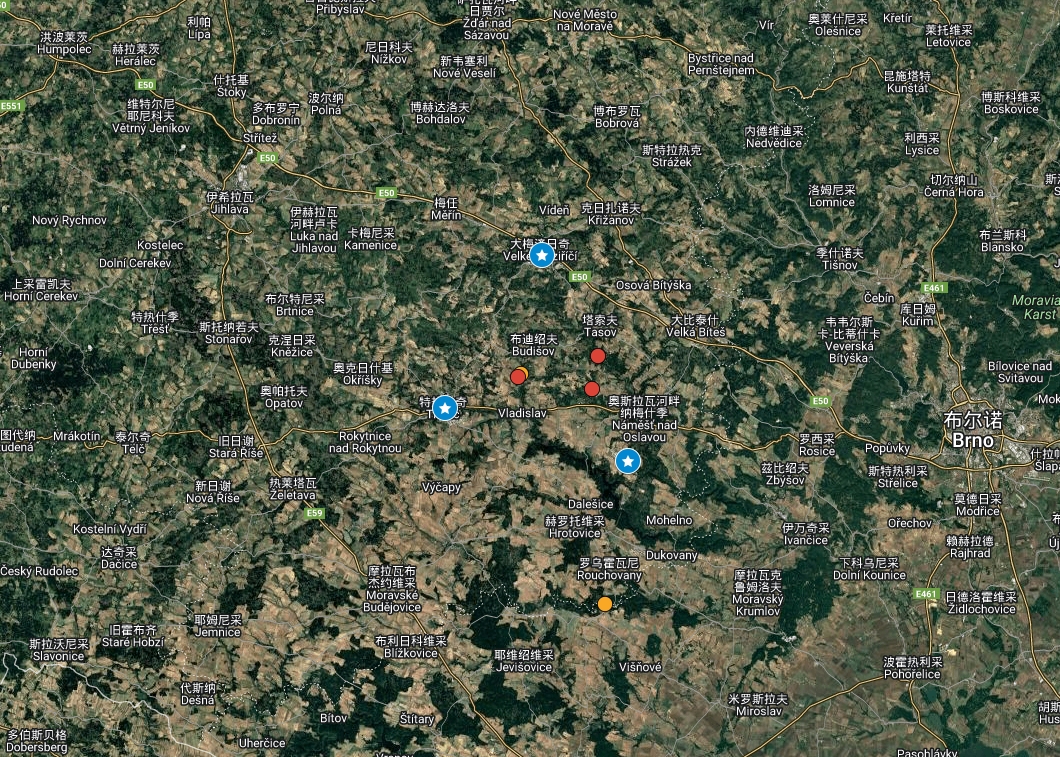
本研究表明,HPAI H5N1 病毒可能通过风传播至 8 公里外。研究结合遗传学、动物流行病学、气象学和地理数据,重构了疫情暴发的时间线,将病毒扩散与风向和风速关联。2024 年 2 月 4 日,捷克共和国某大型养鸭场(B场)的 5 万只育肥鸭中突然出现约 800 只死亡案例。两天后,死亡数激增至 5000 只。该农场毗邻一处常有野生鸟类栖息的湖泊。
为控制疫情,该鸭群被扑杀,并设立了 10 公里的监测区和 3 公里的保护区。然而,2024 年 2 月 12 日,监测区内的两座养鸡场(C1 和 C2)暴发 HPAI 疫情。C1 和 C2 各含两栋鸡舍,鸡群饲养于无垫料的室内笼中。
由于位于监测区内,两农场于 2 月 7 日投喂了增强免疫的营养补充剂。值得注意的是,在疫情暴发前一周,两农场的饲料和饮水消耗量逐渐下降。这一现象最初归因于补充剂,但研究指出其与病程缓慢及潜伏期延长的特征一致。HPAI 最初在 C1 的 A 栋(C1A)和 C2 的 B 栋(C2B)检测到,死亡数略有上升。
值得注意的是,感染和死亡案例集中发生于靠近进气口的区域。这一空间分布表明,通过通风系统进入的污染空气可能促进了疾病传播。为保护 C1B 栋内约 2000 只重要基因储备鸡群,C1A 栋被扑杀。但 C1B 栋最终仍未能幸免,而 C2A 栋全程未受影响。
研究人员通过全基因组测序(WGS)和系统发育分析,揭示了受感染农场间的关联。共获得 38 个 H5N1 基因组,其中 9 个来自 B 场,5 个来自 C2B 栋,3 个来自 C1A 栋,15 个来自 C1B 栋,6 个来自 B 场附近的后院禽群。所有 H5N1 毒株均属 DI 基因型,属于同一亚支。B 场的 3 个毒株与 C1A 栋及 C1B 栋的首例毒株核苷酸序列完全一致。
相比之下,C1B 和 C2B 栋后期毒株呈现农场特异性聚集。此外,B 场附近后院禽群的毒株与 C1A、C1B 首例及 B 场毒株高度相关。中位连接网络分析显示,除一个 B 场毒株外,其余早期 C1 毒株与 B 场毒株形成核心节点,并分出三支:一支为 C1B 特异性簇,一支为 C2B 特异性簇,第三支代表后院禽群毒株。
这一遗传重叠表明病毒存在共同起源,B 场可能是向 C1 和 C2 传播的源头。鸭场与鸡场相距 8 公里,且面向不同市场。对农场经理和兽医的访谈显示,B 场与 C 场之间无直接接触。

图:被感染的场所。在农场 B(a),C1(b)和 C2(c)上的受影响房屋的布局。在 C1 和 C2 上,隧道通风系统气流用橙色箭头表示,用于流出和蓝色箭头。
因此,通过人员从 B 场传播至 C1/C2 或 C1 传播至 C2 的可能性被排除。研究还排除了野生鸟类、啮齿动物和昆虫媒介等其他潜在传播途径。鸡场的封闭式设计及当地缺乏大型水体,进一步降低了野生鸟类传播的可能性。
所有农场海拔相近(408-448 米)。疫情暴发期间天气以少雨、间歇性日照和多云为主,平均湿度 77%-81%。除 2 月 7 日和 8 日夜间外,气温均不低于 6℃。风速数据显示,关键传播窗口为 2 月 4 日中午至 2 月 5 日午夜,持续西南或西风,风速最高达 10 米/秒,与推断的感染路径吻合。
研究结论
气溶胶病毒颗粒而非灰尘是传播关键——研究挑战了“扑杀产生的灰尘是主要空气传播风险”的传统观点,指出感染禽群扑杀前释放的细颗粒气溶胶更具威胁。
此次 HPAI H5N1 疫情始于 2024 年 2 月 4 日的鸭场。尽管源头不明,但附近湖泊的绿头鸭最可能是初始宿主。邻近后院禽群感染遗传相似毒株,表明野生鸟类维持了病毒在当地的循环。
结合事件时间线与风速、风向数据,传播窗口为 2 月 4 日至 9 日,高峰期可能在 2 月 4 日至 5 日。这一结论基于三点:
1)疫情进展缓慢,潜伏期长,表现为症状出现前饲料和饮水摄入减少;
2)感染禽类集中于靠近进气口的区域;
3)供体与受体农场毒株的遗传一致性。
实地调查排除了此期间其他潜在传播途径。研究尤其挑战了“扑杀产生的灰尘是主要空气传播风险”的长期观点,提出感染禽群存活期间释放的细颗粒气溶胶随风传播可能更为关键。
因此,C1B 和 C1A 的首例毒株可能是由 B 场经风传播的初始毒株,随后在本地进化形成农场特异性簇。综合气象、地理、动物流行病学和临床因素,风媒传播是此次疫情扩散的最合理解释。
这些发现强调,未来疫情防控需重视风媒传播风险,特别是在高密度禽类养殖场及依赖机械通风系统的农场中。
期刊参考
Preliminary scientific report. Nagy A, Černíková L, Sedlák K. Genetic data and meteorological conditions: unraveling the windborne transmission of H5N1 high-pathogenicity avian influenza between commercial poultry outbreaks. bioRxiv, 2025, DOI: 10.1101/2025.02.12.637829, https://www.biorxiv.org/content/10.1101/2025.02.12.637829v1
延展阅读
牛H5N1流感显示出通过关键突变使人类适应的潜力
H5N1禽流感蔓延到马身上,引发了对新病毒菌株的担忧